La cornée
La cornée est la partie transparente de l’oeil situé en avant de celui-ci. Elle est constituée de 3 couches : l’épithélium; le stroma et l’endothélium. La greffe de cornée consiste à remplacer la partie de la cornée malade par une cornée saine d’un donneur décédé. La kératoplastie (nom médical de la greffe de cornée) est une chirurgie ophtalmologique qui permet à de nombreux patients de retrouver une bonne vision alors qu’ils étaient porteurs d’une opacité de la cornée ou d’une déformation de la cornée qui les rendaient, sinon aveugles, du moins malvoyants.

Prise en charge

Traitement
Le type de chirurgie sera à adapter à votre pathologie.
La tendance actuelle est de changer uniquement la partie malade de la cornée et de plus en plus rarement toute la cornée comme auparavant. De nombreuses techniques opératoires de kératoplastie (= greffe de cornée) existent. Lors de la rencontre avec votre chirurgien, celui-ci vous expliquera la technique la plus adaptée à votre cas

Suites opératoires d'une greffe de cornée
L’intervention nécessite une hospitalisation courte (en général une nuit) qui sera suivie d’une surveillance rapprochée.
L’activité du patient sera réduite pendant les premières semaines car la cicatrisation doit s’effectuer avant d’envisager une activité normale. Il y a une période d’observation de plusieurs mois. Les soins locaux sont réduits à l’instillation de gouttes.Certains sports seront interdits définitivement à cause du risque élevé de traumatisme (boxe, rugby par exemple). Petit à petit les contrôles s’espaceront et le patient ne sera revu qu’une fois par an si tout va bien. Dans la très grande majorité des cas l’oeil opéré est peu ou pas douloureux. La récupération visuelle est progressive.
Le suivi sera effectué par le chirurgien qui réalise l’ensemble des greffes de notre centre. Si celui-ci est absent, l’ensemble de l’équipe médicale pourra vous prendre en charge. Un suivi médical des patients opérés est primordial en urgence dans les greffes. Tout retard de prise en charge peut être préjudiciable. Il convient de consulter en urgence si l’œil devient douloureux, si l’œil devient rouge ou si vous présentez une baisse de vision. Ces signes peuvent être liés à un début de rejet qui dans la plupart des cas est rattrapable si il est pris tôt. Il faut se souvenir qu’un oeil greffé sera pour toujours un oeil plus fragile nécessitant une surveillance régulière.
L’ablation des fils de suture peut être nécessaire, celle-ci est alors effectuée en consultation.

Résultats
Les résultats sont fonctions des maladies oculaires et de la technique utilisé : le mieux est d’en parler à votre ophtalmologiste.

Complications
Les complications graves de l’opération sont assez rares fort heureusement.
Il convient tout de même de bien être au courant des complications avant une chirurgie.
Le rejet est la principale complication de la greffe de cornée. La fréquence varie entre 10% à 50% de rejets selon le type de pathologie qui a nécessité la greffe et le type de greffe (les greffes lamellaires antérieures et les greffes lamellaires postérieures font moins de rejet que les greffes transfixiantes). Il se manifeste à partir des premières semaines après l’opération et jusqu’à 20 ans après celle-ci. Il peut être traité par des médicaments avec une certaine efficacité. En cas d’échec de ce traitement le greffon reste opaque et la vision est très basse. Une seconde greffe est possible mais son risque d’échec est augmenté.
Comme autres complications on note :
- Les infections qui touchent 2 à 5 cas sur 1000
- L’augmentation de la pression oculaire
- Le traumatisme de l’oeil par le patient ou son entourage
- La déformation de la cornée greffée (astigmatisme) est fréquent pour la greffe transifixiante, à peu près équivalente pour la greffe lamellaire profonde et est presque nulle pour la greffe par DSAEK
- L’oedème rétinien central.

Techniques d'avenir pour la greffe de cornée
Des essais de kératoplastie transfixiante (greffe de cornée classique) sans sutures sont en cours et déjà publiées sur des yeux de porc mais cela reste encore du domaine du rêve en pratique clinique.
Des cornées de culture sont en cours de développement mais ne sont pas encore disponibles.
Différentes kératoplasties
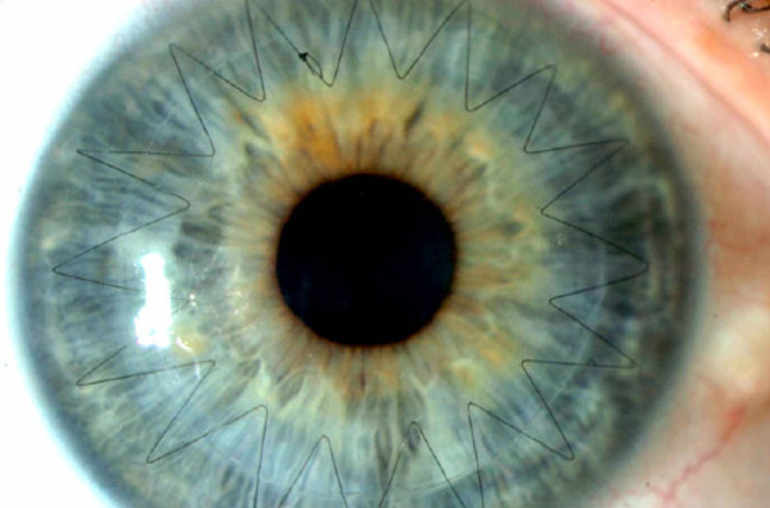
- la kératoplastie transfixiante (KT) qui permet le changement de toute l’épaisseur de la cornée
- la Photo Kératectomie Thérapeutique (PTK) qui permet de traiter une cornée au laser jusqu’à 100 µ ;
- la Kératoplastie Lamellaire Automatisée (ALTK) qui permet de traiter des lésions jusqu’à 250 µ pour la technique dite superficielle et des lésions de toute l’épaisseur de la cornée pour la technique dite profonde ;
- la Kératoplastie Lamellaire Antérieure Profonde (KLAP) qui permet de traiter des lésions jusqu’à la membrane de Descemet ;
- la Kératoplastie Lamellaire Postérieure (DSAEK et DMEK) et l’Endokératoplastie (EKP) qui permettent de traiter les pathologies endothéliales.
Actuellement il existe une forte augmentation de la proportion de chirurgie lamellaire antérieure et postérieure.
1- La kératoplastie transifixiante classique (KT)

La kératoplastie transifixiante classique (KT)
Il s’agit de la technique de référence, très largement la plus utilisée puisque les autres techniques sont de développement récent et pratiquées par encore peu d’équipe. Elle consiste en une trépanation de toute l’épaisseur cornéenne et en une suture d’un greffon comprenant un stroma et un endothélium.
Elle permet de traiter l’ensemble des atteintes de la cornée relevant d’une kératoplastie.
Il s’agit d’une technique ancienne, éprouvée et rapide (1/2 heure) et reste encore une technique pouvant être proposée au patient même dans les indications relevant des autres techniques chirurgicales. Le devenir du greffon sur le long terme est bien connu ce qui en fait une chirurgie prévisible.
Toutefois, on lui reproche de traiter des zones saines alors que de nombreuses atteintes cornéennes touchent juste une partie de la cornée. Par exemple pourquoi remplacer un endothélium dans une opacité cornéenne stromale ou une dystrophie sous épithéliale ? Il s’agit de plus d’une technique de chirurgie à globe ouvert, ce qui lui fait préférer parfois une technique à globe fermé, limitant ainsi les problèmes infectieux et pressionnels post-opératoires. Les résultats réfractifs restent parfois aléatoires : globalement : 50 à 70% des patients récupèrent une acuité >= 5/10ème. On peut considérer que le taux de survie du greffon est de 80% à 1 an et proche de 50% à 5 et 10 ans.
2-Les kératoplasties automatisées (ALTK et AMK)

• La kératoplastie Lamellaire Automatisée (ALTK)
Cette technique chirurgicale dérivée du LASIK permet d’effectuer à l’aide d’un microkératome ou d’un laser Femtoseconde une découpe lamellaire avec un capot libre de la cornée réceptrice et du greffon.
Ce dernier remplacera le capot libre sur la cornée du receveur. Comme les cornées sont disponibles en France uniquement avec une collerette de sclère, on utilise une chambre antérieure artificielle qui permet de maintenir le greffon afin d’effectuer la trépanation. Le capot est ensuite soit suturé, soit collé à l’aide d’une colle tissulaire sur l’œil receveur.
L’ALTK permet théoriquement de traiter des opacités situées dans le stroma antérieur et la partie antérieure du stroma moyen (250µ). En pratique, il est nécessaire d’avoir un endothélium normal et une épaisseur cornéenne régulière. En effet lorsque la cornée réceptrice a une épaisseur variable, le microkératome suit les irrégularités qui sont reproduites au niveau du stroma résiduel. Ainsi, les dystrophies cornéennes héréditaires antérieures sont l’indication idéale de cette chirurgie et cela élimine les kératocônes, les complications d’ulcère et les opacités post-traumatiques.
Au crédit de cette technique, il est indéniable que la facilité de réalisation est importante. Cependant les indications restreintes et la nécessité d’une chambre antérieure artificielle en font une technique peu développée.
• Les Kératoplasties Transfixiantes Automatisées : La greffe de cornée au laser femtoseconde
Il s’agit de techniques de description récente. On utilise pour cela un découpe de la cornée et du greffon à l’aide d’un laser femtoseconde présent à la clinique depuis 2008.
Cela permet ainsi de traiter des pathologies de toute l’épaisseur cornéenne en enlevant un minimum d’endothélium sur la cornée réceptrice. La cornée peut être aussi enlevée en deux temps avec une ablation selon une forme bien précise : (en champignon, tophat, en Z…) Toutes les possibilités sont envisageable. Il s’agit toutefois de variantes dont l’intérêt est à démontrer.
On peut toutefois espérer avec des découpes laser femtoseconde de la cornée :
- un résultat visuel meilleur par une découpe plus précise et plus reproductible
- une ablation plus précoce des fils
Le gros problème de ces chirurgies est le surcoût de la technique sans intérêt important prouvé pour le patient pour l’instant.
3- La kératoplastie lamellaire antérieure profonde (KLAP)

La kératoplastie lamellaire antérieure profonde (KLAP)
Il s’agit d’une technique chirurgicale ancienne décrite par Muhlbauer en 1840 qui est actuellement en net regain d’intérêt.
Au cours de cette procédure l’ensemble du stroma cornéen doit être entièrement retiré pour ne laisser que la seule membrane de Descemet et l’endothélium. Dans un premier temps, on effectue une trépanation des 2/3 ou des 3/4 de l’épaisseur cornéenne. L’étape suivante est de loin la plus difficile et consiste en une dissection manuelle du stroma cornéen jusqu’à la membrane de Descemet. On s’aidera pour cela d’injection dans le stroma d’air, de fluide ou de substance viscoélastique. On effectue enfin une suture classique du greffon débarrassé de sa membrane de Descemet et de son endothélium.
Théoriquement, la KLAP permet de traiter toutes les pathologies cornéennes non endothéliales qui étaient auparavant traitée par Kératoplastie Transfixiante.
Puisqu’il s’agit d’une chirurgie préservant l’endothélium du receveur cela fait théoriquement disparaître le risque de rejet endothélial. Par ailleurs, puisqu’il s’agit d’une chirurgie à globe fermé, on diminue le risque d’endophtalmie et d’hypertonie post-opératoire. Reste encore à évaluer le pronostic sur l’endothélium à long terme. Cette technique permet de plus d’utiliser des greffons cornéens dont la qualité endothéliale serait insuffisante pour une greffe transfixiante permettant ainsi d’améliorer la rentabilité des greffes de cornée.
Il s’agit toutefois d’une chirurgie difficile avec des complications spécifiques qui ne s’observent pas en kératoplastie transfixiante : double chambre antérieure post opératoire (absence d’adhérence de la membrane de Descemet au greffon), opacités profondes au niveau de l’interface entre le greffon et la dissection pré-descemétique, perforation per-opératoire (9-39%).
Les études comparant la kératoplastie lamellaire profonde et la kératoplastie transfixiante rapportent en règle peu de différences réfractives entre les deux techniques. Si le taux de perte cellulaire reste proche ou identique à celui d’un endothélium sain, on peut espérer une survie de plusieurs décennies de la greffe. Cette technique deviendra alors de façon évidente préférable chez le sujet jeune (kératocône).
Cette chirurgie consiste à greffer uniquement la partie antérieure de la cornée (le stroma) qui est malade dans le kératocône et laisse en place la partie postérieure qui est saine (l’endothélium). Grâce à cette technique, il existe moins de rejet et la survie de la greffe est plus prolongée. Il s’agit d’une chirurgie beaucoup plus lourde que les anneaux et le cross linking qui nécessite une hospitalisation. Comme toute greffe, il existe un risque de rejet même des années après l’intervention. Comme après toute greffe, il convient de consulter en urgence en cas d’oeil rouge ou douloureux.
Cette technique lamellaire est réalisée à l’institut depuis début 2006 en pratique courante remplaçant la greffe de cornée classique qui était réalisée auparavant. Actuellement, en raison des progrès dans la prise en charge du kératocône, on considère que seul 1 kératocône sur 100 aura besoin d’une greffe de cornée si il est bien pris en charge.
Le kératocône

Le kératocône correspond à une déformation de la cornée (le revêtement transparent de l’iris et de la pupille de l’oeil) qui s’amincit progressivement, perd sa forme sphérique normale et prend une forme de cône irrégulier. En effet, le mot kératocône, d’origine grecque, signifie «cornée conique». Cette déformation, survenant souvent vers la fin de l’adolescence, engendre des troubles de la vision (vue brouillée et déformée et mauvaise vision de loin) qui nécessitent le port de lentilles spécialisées. Le kératocône atteint généralement les deux yeux, mais pas avec la même sévérité. Le kératocône qui n’est pas contagieux est une pathologie oculaire non inflammatoire.

Fréquence du kératocône
Il y a d’importantes discordances dans les estimations du nombre de personnes atteintes de kératocône, mais beaucoup d’études estiment que la prévalence (nombre de cas dans une population donnée à un moment précis) est comprise entre 1 personne sur 2000 et 1 sur 500. Les variations sont dues aux différents critères diagnostiques et méthodes de détection,certaines formes légères de kératocône pouvant passer inaperçues. En outre, si elle est souvent isolée, cette déformation oculaire peut être associée à d’autres maladies plus complexes.

Population atteinte
Le kératocône touche indifféremment les personnes des deux sexes, quelle que soit leur origine géographique, même s’il semble que les Asiatiques et les patients du Maghreb soient plus affectés. Le kératocône est habituellement découvert à la puberté (entre 10 et 20 ans), mais il peut survenir à tout âge (82 % des cas débutent toutefois avant 40 ans).

Les causes
La cornée est la lentille transparente à travers laquelle on perçoit l’iris coloré et la pupille noire centrale. Normalement, la cornée a une forme arrondie régulière.
Chez les personnes ayant un kératocône, le centre de la cornée s’amincit et forme une protubérance conique et irrégulière qui perturbe la vision. On ne connaît pas encore les causes exactes du kératocône, mais il s’agit probablement d’une maladie génétique : même si aucun gène spécifique n’a été, à ce jour, identifié, le fait que plusieurs membres d’une même famille puissent être atteints et que la maladie se développe presque systématiquement dans les deux yeux appuie la thèse d’une implication génétique. Une recherche est actuellement en cours pour identifier le ou les éventuel(s) gène(s) impliqué(s). En plus de la susceptibilité génétique, des facteurs environnementaux sont nécessaires à l’apparition des symptômes cliniques de la maladie. Les contraintes mécaniques (comme le fait de se frotter les yeux ou encore le port de lentilles de contact) pourraient par exemple contribuer à déclencher la maladie. Comme le kératocône apparaît après la puberté, des hormones pourraient aussi être en cause.
En outre, il se trouve que beaucoup de patients souffrant de kératocône ont une prédisposition aux allergies, et développent souvent un eczéma et/ou une conjonctivite allergique. Il semble donc qu’il existe un lien entre allergie et kératocône dont les mécanismes ne sont pas clairement établis.
Par ailleurs, le kératocône survient souvent chez des personnes ayant une autre maladie, génétique ou ophtalmologique, comme par exemple le syndrome de Marfan, la trisomie 21, la rétinite pigmentaire ou l’amaurose congénitale de Leber (maladie familiale grave des yeux). Ainsi, 5 à 6 % des personnes trisomiques présentent un kératocône. Récemment il a été trouvé une corrélation avec le diabète avec une atteinte plus fréquente et plus sévère dans la diabète de type 2 (non insulinodépendant). On ne sait pas si ces maladies ont des caractéristiques génétiques favorisant la survenue du kératocône, ou si elles sont directement impliquées dans la pathologie.
Au total : Actuellement, tout le monde s’accorde pour retenir une origine multifactorielle associant tout à la fois une cause génétique à laquelle s’associe un certain nombre de cascades biochimiques au sein du stroma cornéen impliquant une production déréglée d’enzyme de dégradation (métalloprotéinases) et une dérégulation du système oxydatif. Le rôle dufrottement mécanique de l’oeil par le patient, souvent par ailleurs allergique paraît également important.
Les symptômes

Les effets du kératocône varient selon les individus et peuvent être de légers à graves. Le plus souvent, les deux yeux sont touchés (dans 90 % des cas) mais il est fréquent que le kératocône ne soit diagnostiqué que d’un seul coté, le délai d’apparition dans le deuxième oeil étant très variable et pouvant atteindre plusieurs années.
Dans les premiers stades, le kératocône entraîne une vision floue (sensation de brouillard) et déformée (astigmatisme). Cette baisse de l’acuité visuelle est surtout ressentie en vision de loin (myopie) et est souvent associée à une sensibilité excessive à la lumière (photophobie), à un éblouissement et à une irritation oculaire (yeux larmoyants). À mesure que le kératocône évolue, l’astigmatisme et la myopie s’accentuent. Comme la déformation de la cornée est irrégulière, la vision subit une grande distorsion. La vue est brouillée, comparable à ce qu’on voit derrière une vitre quand il pleut beaucoup. Les images peuvent même paraître dédoublées ou multiples.
Les personnes atteintes de kératocône doivent changer souvent de lunettes, car celles-ci deviennent vite impuissantes à corriger l’astigmatisme. Dans les stades avancés, la cornée se déforme et s’amincit tellement que des cicatrices apparaissent et l’opacifient, rendant la vision d’autant plus trouble. Mais comme l’évolution peut s’arrêter à tout moment, beaucoup de patients atteints de kératocône n’atteignent pas un tel stade.

Comment fait-on le diagnostic de kératocône ?
Votre ophtalmologiste réalise à son cabinet une consultation de contrôle de la vue et retrouve des paramètres de correction optique inhabituels. Il réalise alors ou fait réaliser une topographie cornéenne (Pentacam, Orbscan…). Celle-ci permet de faire la diagnostic de la maladie car le résultat est spécifique.
Cet examen permet en outre la classification du kératocône d’après Krumeich ; celle-ci est la plus utilisée
- Stade 1 : Myopie et/ou astigmatisme <=5 Dioptries Puissance cornéenne <= 48 Dioptries Stries de Vogt
- Stade 2 : Myopie et/ou astigmatisme >5 <=8 Puissance cornéenne <=53 dioptries Pachymétrie >400 µm
- Stade 3 : Myopie et/ou astigmatisme >8 <=10 Puissance cornéenne >53 dioptries Pachymétrie >200 µm
Stade 4 : Réfraction non mesurable Puissance cornéenne >55 dioptries
Opacité cornéenne
Pachymétrie <200 µm
Il existe une classification plus récente : la classification de BELIN ABCD qui tient compte des donnée de la face postérieure de la cornée. En outre elle pour avantage d’être intégrée directement dans la plateforme Pentacam. Celle-ci inclut des données tomographiques telles que le rayon de courbure antérieure et postérieure des 3mm autour du point le plus fin, la pachymétrie minimale, mais également l’acuité visuelle mesurée. Elle permet ainsi de manière automatisée de documenter les modifications significatives et d’évaluer l’efficacité d’un traitement tel que le cross-linking.
Nouveautés dans le diagnostic
L’analyseur de la viscoélasticité cornéenne
Cet appareil, appelé l’ORA (Ocular Response Analyseur – Reicherts), permet de mesurer la visco-élasticité de la cornée (hystérésie cornéenne) qui pour le cas des kératocônes est abaissée. Il présente peut-être un intérêt pour le dépistage des formes infra-cliniques. Les résultats sont encore en phase d’évaluation mais l’examen est très simple (un petit jet d’air) et les résultats plutôt prometteurs. L’institut dispose actuellement de ce dispositif pour son évaluation clinique.

Evolution
Le kératocône, souvent découvert à la puberté, évolue généralement jusqu’à l’âge de 30-40 ans avant de se stabiliser.
L’évolution est irrégulière, certains kératocônes restant stables pendant quelques années, d’autres s’aggravant puis se stabilisant à nouveau. Les kératocônes peuvent arrêter de progresser à n’importe quel stade. Les stades d’évolution peuvent être classés selon différents critères, mais on distingue souvent 4 stades de gravité croissante allant du kératocône débutant au stade 1 jusqu’au kératocône avec une opacité sur la cornée au stade 4 (voir classification ci-dessus).
Dans de rares cas (moins de 3 %), une complication particulière, le kératocône aigu (« hydrops ») peut survenir.
L’évolution d’un stade au suivant n’est pas obligatoire et n’est pas linéaire dans le temps. Elle est souvent difficilement prévisible et asymétrique (seulement 13% des cas sont unilatéraux). Certains patients présentent donc des formes sévères et rapidement progressives, d’autres gardent toute leur vie une forme fruste et isolée.
Il est important de noter que la vitesse d’aggravation de la maladie est accélérée par le patient lui-même lorsqu’il se frotte les yeux fréquemment. De même, toutes les chirurgies réfractives cornéennes (comme le laser Excimer pour corriger la myopie) risquent d’aggraver ou de décompenser la maladie. De ce fait, elles sont strictement contre-indiquées pour cette affection.
Traitement du kératocône

Axes de traitements
NE PAS SE FROTTER LES YEUX est un recommandation essentielle dans le kératocone car il existe un effet mécanique qui favorise l’évolution de la maladie en déformant la cornée.
Il existe 2 axes de traitement du kératocone : stabiliser le kératocone et améliorer la vision :
- Pour stabiliser la vision il convient de discuter la réalisation d’un « cross linking cornéen »
- POUR AMELIORER LA VISION DANS LE KERATOCONE : La chronologie habituelle de prise en charge thérapeutique comporte dans un premier temps un équipement en lunettes puis, en cas d’échec, une adaptation en lentilles de contact. Finalement, en cas d’intolérance ou si la vision reste insuffisante, le recours à la chirurgie cornéenne s’impose.
Cette dernière comporte deux options :
- les cas les plus favorables peuvent bénéficier de la mise en place d’anneaux intra-cornéens.
- les cas plus sévères impliquent la réalisation d’une greffe de cornée.
Pour donner un ordre de grandeur, environ 10% des patients porteur d’un kératocône reconnu ne seront jamais demandeurs de thérapeutique, 15% seront équipés en lunettes uniquement, 50 % seront équipés en lentilles de contact et 25% bénéficieront d’une chirurgie. Seuls 1% des kératocônes vont bénéficier d’une greffe de cornée.
Les lentilles sont donc l’arme de choix pour la majorité des patients atteints de kératocônes. L’adaptation est cependant délicate voire impossible dans certains cas. Il vaut mieux demander à voir un spécialiste de l’adaptation en lentilles (contactologue) et si possible en lentilles pour kératocône. L’avantage de la lentille de contact par rapport aux lunettes est lié à l’interface qu’elle crée avec le film lacrymal. Cette dernière permet de gommer une grande partie des irrégularités de la cornée. Les lentilles rigides sont beaucoup plus efficaces mais plus complexes à adapter. Lorsque la lentille n’est pas ou plus tolérée, il est licite de proposer une alternative chirurgicale.
Pour les 1% des kératocones pour lesquels la greffe devient nécessaire : Jusqu’à il y a peu de temps seule la chirurgie par greffe de cornée transfixiante était proposée. On devait alors effectuer un changement total de la cornée en mettant en place un greffon issu d’un donneur décédé. Depuis quelques années la chirurgie a fortement évoluée.
Nous allons détailler les 5 nouvelles techniques qui sont maintenant proposées en pratique courante :
- le cross linking cornéen,
- la mise en place d’anneaux intra-cornéens
- la kératoplastie lamellaire antérieure.
- la photoablation du kératocone au laser excimer guidée par la topographie
- La procédure Keraflex

Cross linking cornéen conventionnel à la riboflavine (Ricrolin) (Parfois appelée la photothérapie UVA)
Le cross linking cornéen est un traitement cornéoplastique des kératocônes par modification du collagène cornéen. Ce traitement permet de stopper l’évolution du kératocône.
Il repose sur une photopolymérisation des fibres collagènes par action d’un rayonnement ultraviolet sur une cornée préalablement imprégnée de riboflavine isotonique à 1% ou vitamine B2 (Ricrolin®). Ce geste chirurgical est proposé sous simple anesthésie topique (anesthésie par gouttes). Il consiste à imprégner la cornée de riboflavine (une goutte par minute pendant 20 minutes puis d’éclairer l’œil par une lampe calibrée à UVA (370 nm) pendant 30 minutes. Le geste dure 1 heure est totalement indolore. On met en place une lentille en fin d’intervention et le patient peut ensuite repartir chez lui après un contrôle médical. Les indications sont les kératocônes pas trop évolués (sans opacité centrale et avec une épaisseur cornéenne supérieure à 400microns) qui sont en cours d’évolution (2 examens séparés de 6 mois sont nécessaire pour le prouver ou un changement certain de correction récent), chez un patient de moins de 40 ans (au delà le kératocône cesse d’évoluer spontanément).
Cette technique est réalisée à l’institut depuis début 2010 en pratique courante. L’institut ophtalmique de Somain est resté longtemps le seul établissement privé de la région équipé du matériel de cross linking. C’est pourquoi nous restons le centre régional avec le plus grand nombre de kératocône pris en charge.
Le Professeur Seiler et son équipe ont mis au point la technique de UV Crosslinking en 1997, à Dresden en Allemagne. Dans une étude clinique, ils ont suivi 26 yeux de 25 patients présentant un kératocône évolutif . Dans tous les cas, un seul œil a été traité, l’autre œil servant de contrôle. La technique du traitement consiste en l’abrasion épithéliale de la partie centrale de la cornée dont la superficie est de 9 mm de diamètre et l’application, durant 10 minutes, d’une solution non-toxique et photosensible : la riboflavine. Ensuite, la cornée est irradiée pendant 30 minutes par des rayons UVA (365 nm).
Cette étude démontre que la progression de la maladie a été stoppée dans tous les cas, aucun effet secondaire iatrogène n’a été observé et les évaluations ne montrent aucun changement au niveau de la densité des cellules épithéliales ou au niveau de la transparence cornéenne. Les valeurs maximales de kératométrie ont été diminuée de 2 dioptries dans 70% des cas et les mesures de l’acuité visuelle la mieux corrigée (BCVA) a augmenté dans 65% des cas. Dans tous les cas, l’épithélium s’est rétablit sans incidents, et une série de topographies pratiquées à 6 mois d’intervalle ne montraient pas de progression de l’ectasie cornéenne pendant la période de suivi post-opératoires (de 1 à 4 ans). Les cornées traitées présentaient une augmentation de leur rigidité, un épaississement des fibres de collagène et une résistance plus élevée à la digestion enzymatique.
D’autres études ont été réalisées, notamment par le Dr. Caporossi et ses collègues en Italie, par le Dr. Kanellopoulos en Grèce ainsi que aux Etats-Unis par le Dr. Boxer Wacher. Les résultats de ces études dont le suivi post-opératoire se sont parfois étalés sur 5 ans, ont également montré que la combinaison de la riboflavine avec l’irradiation par UV est non nuisible et efficace pour augmenter de manière significative la rigidité cornéenne.
Une étude communiqué au symposium européen de Vienne en Autriche par le Professeur Hafezi de Genève rapporte que 90% des enfants détéctés à l’adolescence allaient présenter une progression de leur kératocône. Il semble aujourd’hui conseillé de proposer un traitement par cross linking dès la détection à cet âge avant même l’évolution.
Retenons donc que le cross linking à la riboflavine (Ricrolin) permet de stabiliser le kératocône et est proposé chez les patients avec un kératocône :
- avant 40 ans (après le kératocône se stabilise) s’il est évolutif : prouvé par 2 examens à 6 mois d’intervalle
- dans tous les cas détectés avant 18 ans même si le kératocône n’évolue pas.
- avec une Pachymétrie > 400 en tout point de la cornée en topographie

Quand traiter par cross linking ?
S’il n’existe aujourd’hui aucun consensus pour définir une progression d’un kératocône, les bornes les plus utilisées sont :
- une augmentation de la kératométrie maximale de plus de 1 dioptrie
- une myopisation par augmentation de la cambrure cornéenne retrouvée sur une augmentation de la correction sphérique de plus de 0.5 dioptrie ou une augmentation du cylindre de plus de 1 dioptrie
- la nécessité d’adapter une lentille de contact
- une baisse de l’acuité visuelle (mesurée et rapportée par le patient)
Si un ou plusieurs de ces critères sont remplis sur un intervalle de temps court (6 mois ou moins) cela signifie en général que le kératocône est évolutif et qu’il existe une indication de traitement.
L’enfant est un cas particulier et il est conseillé de traiter systématiquement dès la découverte de la maladie comme cela est expliqué ailleurs dans cet article.

Résultats du cross linking
Les résultats cliniques suggèrent (sans démontrer formellement) la survenue d’une stabilisation (mais pas d’une régression ni guérison) du kératocône.
Le cross linking ne permet donc pas la guérison du kératocône; le recul limité dans le temps de cette technique ne permet pas d’affirmer l’effet stabilisateur du cross linking à long terme. Par ailleurs, il existe de nombreuses formes non évolutives de kératocône, ce qui ne permet pas de conclure forcément à l’efficacité du cross linking en cas de stabilisation après réalisation de cette technique.
Des complications rares du cross linking ont été rapportées : inflammation locale transitoire (haze), infections cornéennes (abcès cornéen), et lésions endothéliales (l’endothélium est la couche la plus profonde de la cornée dont l’atteinte peut causer un œdème irréversible). Dans les cas les plus graves, une fonte stromale (nécrose centrale de la cornée) peut être observée.
Rappelons qu’il existe une technique simple pour éviter de faire progresser un kératocône: convaincre le porteur d’arrêter de se frotter les yeux. Les frottements oculaires répétés et vigoureux sont une cause prouvée d’évolutivité pour le kératocône, qui provoque souvent une envie irrépressible de se frotter les paupières
Plus on est avancé en âge, plus il semble probable qu’un seul traitement suffise. Chez les patients jeunes, le risque de retraitement est plus important. Ceci semble lié au fait que le cross linking cornéen survenant de façon physiologique (naturelle) entre 30 et 40 ans n’a pas encore commencé.

Les nouveaux Cross Linkings cornéens
Actuellement la prise en charge du kératocône évolue fortement avec des nouveaux traitements qui porteront sur l’amélioration de la technique du cross linking, afin d’étendre les indications, réduire les effets indésirables et alléger la procédure. La majeure partie des études vise à s’affranchir de la désépithélialisation, responsable des effets indésirables et de la lourdeur de la procédure. En effet, enlever l’épithélium de la cornée entraîne une douleur post opératoire de quelques jours (2-3 jours) diminuée par l’instillation de collyre et par la mise en place d’une lentille pansement en fin d’intervention. Une autre approche consiste à raccourcir le temps d’exposition.
Le principe du cross linking trans épithélial dans le kératocône (Ricrolin TE)
Le principe du cross linking cornéen transépithélial est de favoriser la diffusion de la Riboflavine en ajoutant à la solution conventionnelle une ou plusieurs molécules qui favorisent le passage à travers l’épithélium. Malheureusement les premiers résultats semblent montrer une diffusion moins homogène que lors de la technique classique. Ce traitement est actuellement recommandé pour les cornées fines qui ne peuvent bénéficier de la technique classique : cette technique de cross linking est en cours d’évaluation chez les patients dont l’épaisseur cornéenne est entre 350 et 400 microns ce qui permet de traiter des stades plus évolués de kératocône (on utilise de la Riboflavine hypotonique Ricrolin TE ® à 0,1%). En effet la technique classique est utilisée dans les cornées supérieures à 400µ. Nous utilisons la technique depuis 2010. Il convient de noter que cette technique reste de façon certaine moins efficace que la technique classique, la Riboflavine dans la cornée est en quantité moins importante et surtout présente dans la partie antérieure de la cornée. Le traitement est dans les études cliniques moins efficace avec un taux d’évolution de plus de 60% des kératocones avec cette technique . Il convient donc à notre avis de la réserver aux cas où il n’est pas possible de faire autrement (les contre indications des autres techniques).
La iontophorèse dans le kératocône (Ricrolin +)
La iontophorèse (de iontos = ions et phoresis= se déplacer à travers de ) est une nouvelle technique non invasive séduisante d’application de la riboflavine sans désépithélialisation (sans douleur). Déjà utilisé en dermatologie, elle consiste à faire pénétrer une molécule chargée à l’aide d’un courant électrique de très faible intensité dans le corps humain (et donc dans la cornée dans le cas présent). Elle permettra de mieux faire pénétrer la riboflavine sans avoir à enlever l’épithélium cornéen grâce à un courant électrique minime appliqué sur l’oeil. La technique est commercialisée au 1er trimestre 2013 en France et nous l’utilisons depuis juin 2013 en pratique courante. En dehors de l’absence de douleur, cette technique diminue les risques d’infection, diminue l’inflammation post opératoire et donc diminue le temps de gêne post opératoire. Cette technique présente aussi le grand intérêt de durer 14 minutes au lieu de 1 heure si on l’associe à une irradiation de forte puissance. (5 minutes d’imprégnation et 9 minutes d’irradiation à 10 mW). Les études expérimentales présentées à la société française d’ophtalmologie montrent que le taux de Riboflavine dans la cornée est moindre par rapport à la technique classique de cross linking. Il est possible que cette technique soit moins efficace que la technique classique mais cette technique permet de limiter les risques et les douleurs liées à la désépithélialisation. Un ratio bénéfice/risque est donc à étudier.
Des résultats encourageants ont été publiés récemment à la Société Française d’ophtalmologie avec un résultat équivalent à un an par rapport à la technique clasique qui est la technique de référence. Il n’y a pas significativement plus d’évolution avec les 2 techniques.
Le cross linking Rapide
Une idée Récente est d’accélérer la procédure de cross linking en augmentant l’intensité de la lumière. En effet selon la loi de Bunsen-Roscoe : l’effet = l’intensité x le temps. Si on augmente l’intensité, on peut ainsi diminuer le temps de traitement. Actuellement avec cette technique, l’imprégnation reste de 20 minutes dans la première phase, par contre la phase de traitement est de 9 minutes au lieu de 30 minutes. Cette technique semble avoir des résultats équivalents même si le recul est plus faible.
Le cross linking Rapide AVREDO
Il s’agit d’une autre nouvelle technique qui est en cours d’évaluation et qui se base sur le même principe d’augmentation de l’intensité lumineuse ((30 mW/cm²) pour diminuer le temps d’exposition (3 minutes). Cette technique est séduisante car elle permet de faire un cross linking beaucoup plus rapidement. Cependant il semble que le traitement soit plus superficiel qu’avec le cross linking classique. Il est possible que cela soit suffisant mais à ce stade les évaluations sont en cours et seul les évaluations à plus long terme et sur un grand nombre de patient permettront de le savoir.
Le cross linking associé au laser Femtoseconde dans la prise en charge du kératocône
Classiquement le cross linking nécessite une désépithélialsation centrale qui est source de douleurs en post opératoire. Kanellopoulos a proposé en Grèce en 2009 une procédure alternative en créant une poche intrastromale (dans l’épaisseur de la cornée) à l’aide d’un Laser Femtoseconde à 100 microns de profondeur. La riboflavine est alors directement injectée dans cette poche puis le protocole traditionnel d’exposition est appliqué. Cela évite ainsi la douleur éventuelle après l’opération. Les résultats précis en comparaison avec la technique de référence n’est pas connu.
Le cross linking sur mesure (customized cross linking)
Les nouvelles techniques d’étude du kératocone permettent de mesurer le module d’élasticité de la cornée en différents points. On a pu ainsi constater qu’en regard du cône, la face antérieure de la cornée était plus faible biomécaniquement. Par contre à distance du cône les caractéristiques biomécaniques de la cornée sont proches de la normale. Cela montre l’intérêt du développement d’un cross linking sur mesure c’est à dire guidé par la cartographie élastographique. Cela permet de prendre en compte l’asymétrie des propriétés biomécaniques de la cornée alors que dans le cross linking standard, l’anisotropie perdure. Ainsi réduire cette asymétrie de propriétés pourrait permettre une interruption plus efficace du cycle de décompensation biomécanique et éventuellement leur régression. Cela reste un axe de recherche et nécessite une comparaison avec les résultats d’un cross linking standard qui reste la référence.

Greffe lamellaire profonde antérieure dans le kératocône
Cette chirurgie consiste à greffer uniquement la partie antérieure de la cornée (le stroma) qui est malade dans le kératocône et laisse en place la partie postérieure qui est saine (l’endothélium). Grâce à cette technique, il existe moins de rejet et la survie de la greffe est plus prolongée. Il s’agit d’une chirurgie beaucoup plus lourde que les anneaux et le cross linking qui nécessite une hospitalisation. Comme toute greffe, il existe un risque de rejet même des années après l’intervention. Comme après toute greffe, il convient de consulter en urgence en cas d’oeil rouge ou douloureux.

Anneaux intracornéens
Il existe des anneaux plus ou moins long, plus ou moins épais. On peut mettre un ou deux anneaux par oeil selon les mesures préopératoires.
Principe des anneaux intracornéens dans le kératocône
Les anneaux sont discutés pour les patients non améliorés ou ne supportant pas les lentilles et qui n’ont pas d’opacité cornéenne centrale. Cette technique est utilisée depuis 1997 mais s’est développée de façon récente grâce à la possibilité de réaliser le tunnel au laser Femtoseconde ce qui la rend très sûre.
Elle permet de retarder la greffe et permet une amélioration significative à moyen et long terme.
Les anneaux intra-cornéens sont des petits segments semi-circulaires rigides en PMMA (plastique). Leur place dans la prise en charge thérapeutique se situe entre l’échec de l’adaptation en lentille et le recours à la greffe de cornée. Ils sont posés pour le kératocône depuis 1997. On introduit les anneaux dans l’épaisseur même de la cornée. Les anneaux intra-cornéens ont pour vocation de la renforcer. Bien positionnés, ils permettent de retendre la cornée centrale. L’importance et l’irrégularité de l’astigmatisme cornéen sont ainsi diminuées.
Deux modèles sont commercialisés :
- les INTACS® (Addition Technology, KeraVision, USA)
- les anneaux de Ferrara® ou les Keraring (Mediphacos, Brésil).
Le retard dans le développement de cette technique chirurgicale a été lié à la difficulté de réaliser un tunnel manuellement pour mettre en place des anneaux intra-cornéens sur une cornée amincie par le kératocône. Cependant l’arrivée du laser Femtoseconde pour la chirurgie de la myopie a rendu simple et automatisée la réalisation d’un tunnel sans risque de perforation. Cette technique est devenue courante actuellement depuis l’arrivée du laser Femtoseconde (nous disposons de ce matériel depuis 2007 à l’institut). Cette technique ne peut pas être proposée aux kératocônes avec une opacité centrale (stade 4) car on ne peut pas espérer d’amélioration visuelle en raison de l’opacité cornéenne qui gêne dans tous les cas la vision.
Résultat des anneaux intracornéens dans le kératocône
Les anneaux permettent de diminuer l’astigmatisme, de diminuer l’équivalent sphérique (myopie le plus souvent) et de diminuer les aberrations optiques. Ils permettent ainsi d’améliorer la meilleure vision après correction et sans correction. Il ne faut pas croire qu’après chirurgie par anneaux la vision se normalise loin de là.
Si on fait un analyse des résultats de 20 études sur les Anneaux comme l’a fait David Pinero, on note une diminution de l’astigmatisme de 0.75 à 2.8 dioptries, de la sphère (myopie) de 2.14 à 9.6 dioptries selon les auteurs. La kératométrie diminuait de 2.14 à 9.6 dioptries selon les auteurs mais la majorité retrouve une diminution entre 2.5 et 4 dioptries. L’acuité visuelle était améliorée dans 60 à 80 % des cas.
Il convient de retenir que le résultat est d’autant meilleur que le kératocône est peu évolué.
P Pena-Garcia a développé en 2012 sur ces bases un modèle mathématique de prédiction des modifications visuelles suite à la mise en place d’anneaux intracornéens. Ce modèle mathématique nous aide à proposer pour chaque patient le meilleur anneau.
Une étude récente présentée par le Dr Assouline au 4 ème congrès international d’Amsterdam en octobre 2013 est intéressante. Il reprend une série de 56 cas d’anneau Keraring ou Intacts posés au Laser femtoseconde. Il s’agissait de kératocônes évolutifs avec intolérance aux lentilles de contact rigides. L’étude montrait la progression durant toute la durée du suivi (4 ans) de l’effet bénéfique des anneaux kéraring pour tous les paramètres étudiés. Cela suggère que les anneaux semblent stabiliser l’évolution du kératocône et que l’effet s’améliore sur le long terme.
Les anneaux intracornéens et le cross linking dans le kératocône
Il est possible d’associer un traitement par anneau intracornéen et un traitement par crosslinking dans le traitement du kératocône. L’association la plus souvent effectuée est de commencer par la mise en place d’anneau pour améliorer la vision puis de bloquer l’évolution et l’efficacité de l’anneau en réalisant un cross linking 3 mois après.
Les anneaux intracornéens et la greffe dans le kératocône
Les anneaux intracornéens n’empêchent pas une greffe de cornée si celle-ci devient nécessaire. En effet le diamètre de la greffe est plus important que celui des anneaux. Le fait de mettre en place des anneaux intracornéens n’est donc pas préjudiciable pour la prise en charge future.

Les implants toriques dans le kératocône (ICL)
Dans de rares cas lorsque l’astigmatisme est stable et pas trop irrégulier mais qu’il est trop important pour être corrigé en lunettes ou lentilles, il est possible de proposer un implant intra-oculaire correcteur. Bien entendu il convient pour cela que la cornée soit encore bien transparente. Cet implant est torique pour corriger l’astigmatisme et la myopie associée dans le même temps. Il est mis en place par le chirurgien derrière l’iris et devant le cristallin. Bien que potentiellement utiles, ces implants sont peu posés mais sont en train de prendre une place plus codifiée dans la prise en charge de la maladie.

Le laser Excimer dans le kératocône
Une autre option de traitement consiste à réaliser une photoablation au laser excimer guidée par la topographie (« topoguidée ») »du kératocône parfois associée au cross linking.
Le principe est de partiellement corriger l’erreur sphérocylindrique myopique et ainsi d’améliorer le confort visuel du patient qui aura besoin d’une correction moins importante. Ce laser pourra être associé à un cross linking pour bloquer cette amélioration. Kanellopoulos a décrit cette technique en 2007. Il a publié en 2009 une étude comparant 127 yeux traités par cross linking puis 6 mois après traités par laser comparé à 198 yeux traités simultanément par laser et cross linking. L’épaisseur de la cornée après traitement ne devait pas être inférieure à 350µ. Il existe une amélioration significativement plus importante dans le groupe traité simultanément :
- de l’acuité visuelle corrigée
- de l’acuité visuelle sans correction
- du haze (inflammation de la cornée) post opératoire
- de l’équivalent sphérique
- de la kératométrie
Le recul moyen était important 36 mois +/- 18 mois (24 à 68 mois).
Il s’agit d’une piste intéressante qui se développe actuellement. De nombreuses études continuent à montrer son intérêt dans les kératocones peu évolués. Nous proposons cette technique actuellement en routine dans notre centre. Il sera intéressant de voir les résultats à plus long terme.

Keraflex dans la prise en charge du kératocône
Une nouvelle procédure de traitement est en cours d’évaluation très récemment et consiste en un applatissement de la cornée en chauffant la cornée à l’aide d’une sonde émettant des micro-ondes de faible énergie en surface de l’oeil créant une « lésion » sur les 150 microns superficiels du stroma sous la membrane de Bowman de l’épithélium. Cette procédure est ensuite suivie d’un »blocage avec un cross linking. Les résultats semblent toutefois être modérés.

Conductive Keratoplasty et kératocône
La « conductive keratoplasty » est une technique utilisée depuis quelques années déjà dans la chirurgie de la presbytie et dans l’hypermétropie faible pour ne plus porter de lunettes. Cette technique utilise des propriétés similaires au kéraflex en chauffant la cornée pour la déformer. Les résultats sont transitoires et des protocoles d’étude sont en cours pour l’associer au cross linking. Cela semble donner des résultats plus durables.

Faut-il faire des chirurgies qui combinent Anneau et Cross linking ?
L’idée est d’associer le cross linking qui stabilise le kératocône à une autre chirurgie qui améliore la vision. Il s’agit là d’un sujet qui n’est pas tranché.
Le but du cross linking est de stabiliser une cornée qui se déforme. Il est alors logique d’associer une technique visant à améliorer l’acuité visuelle par modification de la forme de la cornée stabilisée. Le délai de chirurgie pour mettre des implants est difficile à préciser dans la mesure ou l’effet du cross linking est parfois retardé avec des effets favorables parfois sur plusieurs mois.
Un traitement concomitant Anneau et cross linking soulève des questions :
– Quelle procédure réaliser en premier ? Si la création du tunnel est réalisée d’abord, ne peut-on pas craindre une diffusion de la Riboflavine dans les tunnels et réaliser un cross linking plus postérieur ?
– Est-il logique d’associé 2 techniques imprécises, les résultats devenant ainsi moins prévisibles ?
Il peut alors être logique de réaliser un traitement par Anneau d’abord et un fois le résultat stabilisé et appréciable le « bloquer » par un cross linking.
Chan a publié en 2007 une série d’un anneau intracornéen seul (12 yeux de 9 patients) comparé à un groupe (de 13 yeux de 12 patients ) avec un anneau associé immédiatement à un cross linking sans désépithélialisation ( immédiatement au décours de la mise en place des anneaux). Il semble que les résultats soit meilleurs pour la chirurgie combinée pour les valeurs K max, K moyen, du cylindre et pour l’indice de régularité de surface.
Si on effectue les anneaux et le cross linking, dans quel ordre commencer ? Coskunseven a publié en 2009 une étude qui semble montrer que la mise en place d’anneau après cross linking donnait des moins bons résultats que la mise en place d’anneau avant cross linking.
Nous pouvons voir que le débat n’est pas tranché même si l’approche est séduisante
Adresses de nos sites
Site de Somain - 28, rue Anatole France 59490 Somain
Site de Douai - 11 Avenue des Potiers, 59500 Douai
Site de Valenciennes (Polyclinique Vauban) - 10 Avenue Vauban, 59300 Valenciennes
Site de Cambrai - 20 Rue Alsace Lorraine, 59400 Cambrai
Tel et contact
Consultations : 03 27 99 88 88 ou cliquez-ici
Hospitalisation : 03 27 99 88 99
Fax
Accueil : 03 27 99 88 59
Transports en commun pour venir
A 6 minutes de la gare de Somain
Véhicule personnel
"En voiture : Autoroute A21, sortie 28 Aniche/ Somain"
Contact
Consultations :
03 27 99 88 88
Hospitalisation :
03 27 99 88 99
Accès
Horaires
Accueil ouvert de 8h30 à 17h30 du lundi au vendredi
Fermé le samedi et le dimanche
Visites de 10h30 à 20h


